Schnellere Genesung Corona-Wirkstoff Remdesivir: USA erlauben begrenzten Einsatz
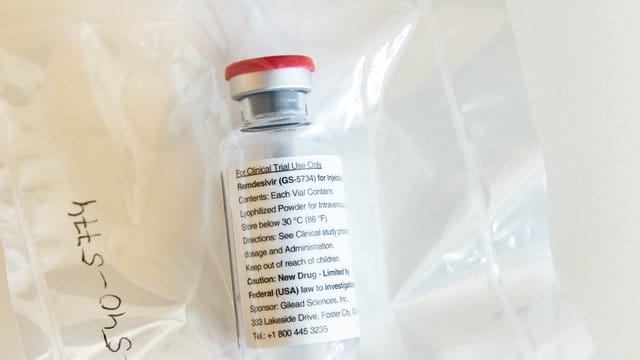

Washington (dpa) - Die USA erlauben den begrenzten Einsatz des Wirkstoffs Remdesivir bei Covid-19-Patienten in Kliniken. Eine klinische Studie hatte zuvor gezeigt, dass der ursprünglich für Ebola entwickelte Wirkstoff bei Covid-Patienten die Zeit bis zu einer Genesung um mehrere Tage verkürzen kann.
Die rasche Zulassung sei extrem ungewöhnlich - und nicht gänzlich unproblematisch, sagen deutsche Experten.
Die Ausnahmegenehmigung sei angesichts der Coronavirus-Pandemie "in Lichtgeschwindigkeit" zustande gekommen, hatte der Chef der US-Lebensmittel- und Arzneimittelbehörde FDA, Stephen Hahn, am Freitag im Weißen Haus gesagt. Präsident Donald Trump bezeichnete den Schritt als "sehr vielversprechend".
Der Chef des Biotech-Unternehmens Gilead, Daniel O'Day, erklärte, das Unternehmen werde US-Behörden 1,5 Millionen Dosen Remdesivir spenden, die für mehr als 100 000 Behandlungen ausreichen sollten. Patienten, die an der Lungenkrankheit Covid-19 litten, könnten das Medikament nun je nach Schwere der Erkrankung fünf oder zehn Tage lang bekommen, erklärte Gilead. Die US-Regierung werde die Verteilung des Medikaments übernehmen, um sicherzustellen, dass es ankomme, wo es am dringendsten gebraucht werde. Bis Dezember wolle man genügend Remdesivir für eine Million Behandlungen produzieren.
Remdesivir ist bislang weltweit nirgendwo als Medikament zugelassen. Die Ausnahmegenehmigung für die USA entspricht keiner formellen Zulassung, was ein wesentlich aufwendigerer Prozess ist. Selbst die Ausstellung einer begrenzten Ausnahmegenehmigung nach nur einer vielversprechenden klinischen Studie ist ungewöhnlich. Bislang gibt es jedoch keine Impfung gegen das neuartige Coronavirus und auch keine zuverlässige zugelassene medikamentöse Therapie.
Am Mittwoch hatte das Nationale Institut für Infektionskrankheiten (NIAID) der USA erklärt, Remdesivir habe im Rahmen einer klinischen Studie die Behandlungsdauer deutlich verkürzt. Institutsleiter Anthony Fauci sprach von einer "signifikanten positiven Wirkung bei der Verringerung der Zeit bis zur Genesung".
Die ungewöhnlich schnelle Erteilung der Ausnahmegenehmigung ist nach Ansicht des deutschen Medizin-Ethikers Peter Dabrock vertretbar. Allerdings müssten wichtige Bedingungen erfüllt sein. So dürften die vorliegenden Daten keine Hinweise darauf geben, dass die Anwendung ohne Nutzen ist, und sie müssten zeigen, dass die Nebenwirkungen akzeptabel sind. Zudem müssten die Patienten oder ihre gesetzlichen Vertreter in die Behandlung einwilligen. "Wenn das gegeben ist, scheint mir die Zulassung in einer weltgesellschaftlichen Notsituation wie dieser verantwortbar zu sein", sagte der ehemalige Vorsitzende des Deutschen Ethikrates.
Als "extrem ungewöhnlich" beurteilt Gerd Fätkenheuer die Entscheidung der US-Zulassungsbehörde. Der Mediziner von der Uniklinik Köln hat den deutschen Teil der Studie geleitet. Aus drei Studienzentren wurden Daten von 13 Patienten zugeliefert. Die Daten der jetzt vorliegenden Zwischenbegutachtung zeigten eine erste Wirkung von Remdesivir, aber wichtige Fragen seien noch offen. So fehlten Angaben zu Nebenwirkungen, und es sei nicht klar, welche Patienten am ehesten von einer Behandlung profitieren. Auch der Einfluss auf die Sterblichkeit sei noch nicht sicher zu beurteilen. "Ich sehe das von daher insgesamt kritisch."
In Deutschland hat das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) Anfang April ein sogenanntes Arzneimittelhärtefallprogramm für Remdesivir bestätigt. Damit dürfen Patienten das noch nicht zugelassene Mittel erhalten. Derzeit habe das BfArM insgesamt vier klinische Prüfungen mit Remdesivir zur Behandlung von Covid-19 genehmigt.
Die US-Studie mit mehr als 1000 Teilnehmern ist nach Angaben der NIAID mit Kontrollgruppen durchgeführt worden, die Datenerhebung hätten unabhängige Experten begleitet. Patienten mit der vom Coronavirus verursachten Lungenkrankheit Covid-19 waren Fauci zufolge nach durchschnittlich 11 Tagen wieder genesen, die Patienten der Kontrollgruppe hingegen erst nach 15 Tagen. Die Resultate müssten noch unabhängig geprüft und veröffentlicht werden, schränkte Fauci ein. Zudem führte das Medikament nur zu einer geringfügig niedrigeren Sterblichkeitsrate.
Eine ebenfalls diese Woche im Fachmagazin "The Lancet" vorgestellte chinesische Studie kam hingegen zu dem Schluss, dass sich der Zustand der Patienten mit Remdesivir nicht wesentlich verbessert. Aus Patientenmangel wurde diese Studie allerdings frühzeitig abgebrochen. Zudem waren die meisten dieser Patienten erst spät im Krankheitsverlauf mit Remdesivir behandelt worden.
Der Wirkstoff hatte zuvor in Laborversuchen einige Wirksamkeit gegen das neuartige Coronavirus Sars-CoV-2 gezeigt. In Tierversuchen wirkte es gegen andere Coronavirus-Infektionen wie Sars und Mers.
Bundeskanzlerin Angela Merkel (CDU) rief am Samstag in ihrer wöchentlichen Videoansprache (Podcast) zu einer internationalen Zusammenarbeit bei der Suche nach Medikamenten und Impfstoffen für die Eindämmung der Pandemie auf. Mit Blick auf die Geberkonferenz am 4. Mai, zu der die EU-Kommission eingeladen hat, kündigte sie an, dass Deutschland sich mit einem "deutlichen finanziellen Beitrag" beteiligen werde. Einen genauen Betrag wollte sie noch nicht nennen.
Wissenschaftler der Johns-Hopkins-Universität in Baltimore haben in den USA inzwischen mehr als 1,1 Millionen Infektionen verzeichnet (Stand Freitagabend) - rund ein Drittel der bestätigten Infektionen weltweit. Die Zahl der Toten in den USA liegt demnach bei mehr als 65 000.

















