Mehr als 150 Journalistinnen und Journalisten berichten rund um die Uhr für Sie über das Geschehen in Deutschland und der Welt.
Zum journalistischen Leitbild von t-online.Vier Phasen kurz erklärt Corona-Impfstoff: Warum dauert die Entwicklung so lange?


Normalerweise dauert es viele Jahre, einen wirksamen und sicheren Impfstoff herzustellen. Beim Coronavirus wird die Forschung deutlich beschleunigt. Ein Überblick von der Analyse bis zur Marktreife.
Es ist eine der großen Fragen der Corona-Pandemie in Deutschland: Wann wird es einen Impfstoff gegen das Virus geben? Doch statt konkreten Antworten gibt es bislang nur Prognosen. Einige Experten rechnen erst im Frühjahr 2021 mit einem Impfstoff – andere halten dies dagegen bereits Ende 2020 für möglich.
Nach Angaben des Verbandes der Forschenden Arzneimittelhersteller (vfa) ist das immens schnell – auch wenn es angesichts der Pandemie als langsam empfunden wird. Denn frühere Impfstoffprojekte dauerten meist zwischen zehn und zwanzig Jahre.
Das bestätigte auch die Virologin Prof. Dr. Marylyn Addo. "Es ist noch nie da gewesen, dass ein Virus im Januar entdeckt wurde und im März dann schon der erste Mensch in einer klinischen Prüfung geimpft wurde. So schnell war die Impfstoffentwicklung noch nie", sagte sie im Interview mit t-online.de.
Generell gilt: Zuerst muss das Virus analysiert und verstanden werden, über welche Mechanismen der Erreger die Immunreaktionen des Körpers auslöst. Erst dann kann mit der Entwicklung eines Impfstoffs begonnen werden. Dessen Prüfung erfolgt in mehreren Phasen.
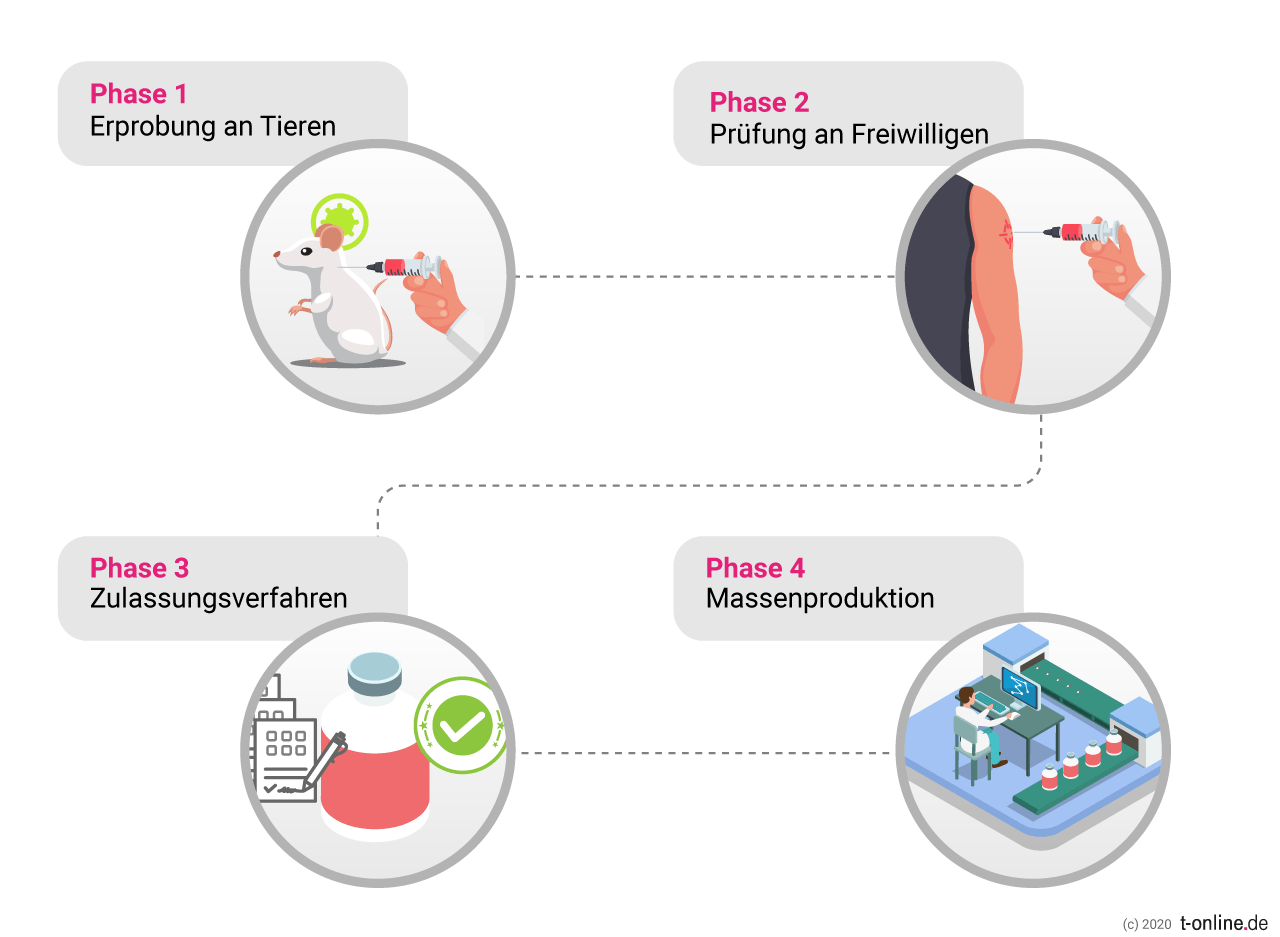
Die vier Phasen der Impfstoffentwicklung
Phase 1: Erprobung an Tieren
In der ersten Phase wird getestet, wie wirksam und verträglich der Impfstoff ist – zunächst an Tieren. Neben Affen nutzen Forscher bei der Entwicklung eines Impfstoffs gegen SARS-CoV-2 auch Frettchen und genetisch veränderte Mäuse.
Phase 2: Klinische Prüfung an Freiwilligen
In Phase 2 finden Studien an freiwillig teilnehmenden Menschen statt., die sich über Monate hinziehen können. Die klinische Prüfung des Wirkstoffs erfolgt in mehreren Etappen:
- An einer kleinen Gruppe freiwilliger gesunder Testpersonen
- An einer größeren Teilnehmergruppe, zu der meist auch Patienten gehören, die an der Krankheit leiden, auf die der potenzielle Wirkstoff ausgerichtet ist
- In einer größeren Studie mit einer repräsentativen Patientengruppe, die oft aus mehreren Tausend Teilnehmern aus verschiedenen Ländern besteht
Phase 3: Zulassungsverfahren
Fallen die Ergebnisse der klinischen Tests aus Phase 2 vielversprechend aus, beantragen die Unternehmen eine Zulassung bei den Behörden. In der aktuellen Corona-Lage kann dieses Verfahren beschleunigt werden, sodass die vorläufigen Ergebnisse begutachtet werden, noch während die Studien laufen. In Deutschland ist das Paul-Ehrlich-Institut (PEI) für die Zulassung von Impfstoffen zuständig.
Phase 4: Massenproduktion
Wird der Impfstoff zugelassen, startet schließlich die Massenproduktion. Um das Verfahren noch weiter zu beschleunigen, beginnen einige Hersteller bereits während der Zulassungsphase mit der Produktion.
Auch nach der Zulassung wird der Impfstoff regelmäßig kontrolliert. Kommt es beispielsweise zu Nebenwirkungen im Zuge einer Impfung, müssen diese an den Hersteller und die zuständigen Behörden gemeldet werden. In Deutschland sind hierfür das Bundesinstitut für Arzneimittel (BfArM) sowie das Paul-Ehrlich-Institut (PEI) zuständig.
- Verband Forschender Arzneimittelhersteller (vfa)
- Eigene Recherche
- Die Informationen ersetzen keine ärztliche Beratung und dürfen daher nicht zur Selbsttherapie verwendet werden.
Quellen anzeigen